
Untersuchung der Flammenfärbung mit dem Spektroskop
Gustav Kirchhoff und Robert Bunsen haben ab 1859 in Heidelberg bei
der Untersuchung der Flammenfärbung entdeckt,
dass jedes Element ein charakteristisches Linienspektrum aussendet.
Natrium
sendet z.B. zwei gelbe Linien aus, die man mit einem Spektroskop betrachten kann.

Flammenfärbung bei Natrium, Foto von A.S.

Spektroskop, Foto von Gaye
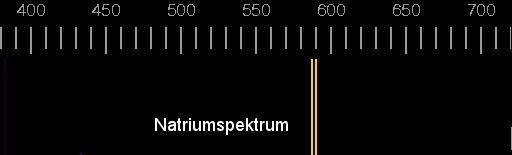
Spektrum des Natriums
Das Spektrum des Wasserstoffatoms
Das Spektrum des Wasserstoffs erzeugten wir mit einer Wasserstofflampe.

Wasserstoff-Gas-Entladungsröhre

Licht der Wasserstoff-Gas-Entladungsröhre
Wir konnten mit dem Spektroskop im Spektrum des Wasserstoffs 4 Linien entdecken. Im Bild des Spektrums, das mit einem sehr genauen Spektrometer aufgenommen wurde, sind sogar 6 Linien erkennbar.
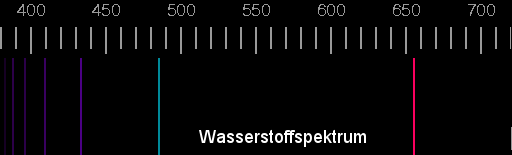
Spektrum des Wasserstoffs
Diese für jedes Element charakteristischen Linien blieben völlig unverstanden. Erst als Bohr sein Atommodell veröffentlichte, wurden sie verstanden.
Das Bohr'sche Atommodell
Das Bohr'sche Atommodell ist eine Weiterentwicklung des Rutherford'schen
Atommodells. Bohr stellte zwei Postulate (Forderungen) auf, mit denen er
die Aussendung von Licht erklären konnte.
1. Postulat:
In einem Atom sind für Elektronen nicht beliebige Bahnen erlaubt, sondern nur
ganz bestimmte. Die erlaubten Bahnen werden von innen nach außen
numeriert. Die Nummer wird Hauptquantenzahl genannt. Die Elektronen
können zwischen den Bahnen hin und her springen.
2. Postulat:
Beim Wechsel eines Elektrons von einer äußeren auf eine innere Bahn
wird Energie in Form von Licht abgestrahlt. Der Betrag der abgestrahlten
Energie entspricht der Energiedifferenz der beiden Bahnen. Je größer dieser
Energiebetrag ist, desto violetter ist das Licht.
Aussendung von Licht nach dem Bohr'schen Atommodell
Elektron (in Gelb), farbiges Licht, Kern und Bahnen
Das Elektron sendet sichtbares Licht aus, wenn es von der sechsten (dunkles Violett), fünften (Violett), vierten (Hellblau) oder dritten (Rot) Bahn auf die zweite Bahn springt.