
Elektrolytische Reinigung von Rohkupfer
Rohkupfer hat einen Reinheitsgrad von bis zu 98%. Der Rest sind andere Metalle z.B. Zinn, Zink, Gold,…
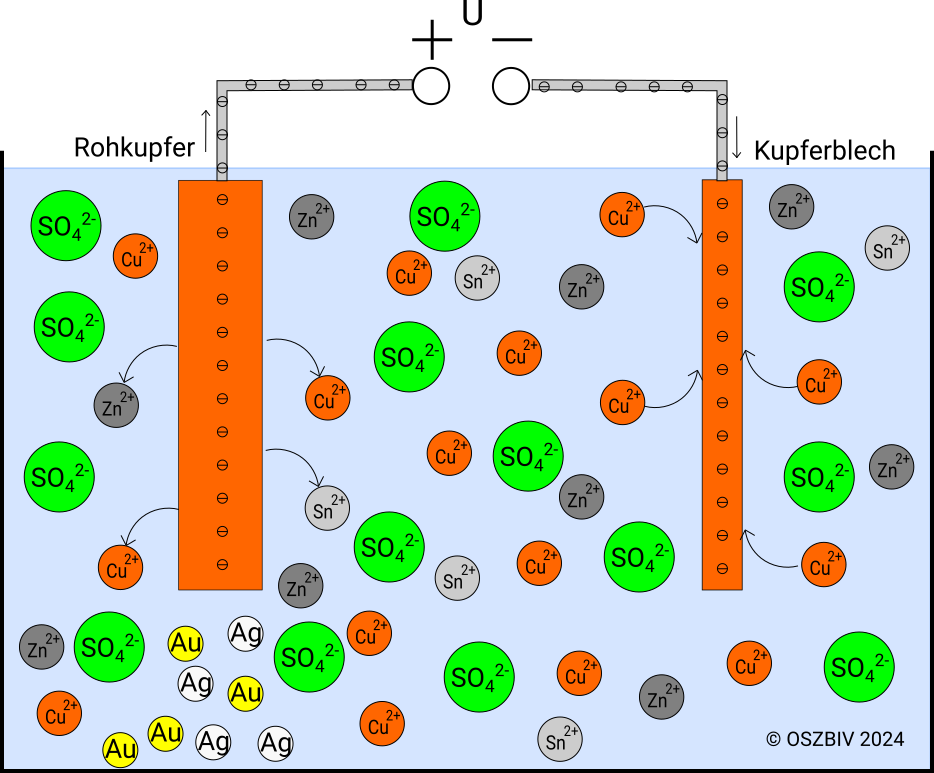
Elektrolytlösung mit Rohkupfer und reinem Kupferblech
Skizze von Herrn Ecker
Am Pluspol werden Kupferatome zu Kupferionen oxidiert.
Cu(s) -> Cu2+(aq) + 2e-
Außerdem werden alle Metalle, die ein niedrigeres Standardpotential besitzen ebenfalls oxidiert.
Die Metalle mit höheren Standardpotential werden nicht oxidiert. Sie sinken auf dem Boden ab und bilden den Anodenschlamm. Dieser Schlamm ist wertvoll, da er Edelmetalle enthält.
Am Minuspol nehmen die Kupferionen zwei Elektronen auf und bilden Kupferatome. Da Kupfer das höchste Standardpotential der Metalle in der Lösung besitzt wird es als einziges aus der Lösung reduziert.
Cu2+(aq) + 2e- -> Cu(s)
Die Metalle mit den niedrigeren Standardpotential bleiben in der Lösung.
Erstellt von Fatima mit kleinen Ergänzungen durch Herrn Ecker 9.1.24